

 当前位置:科研成果
当前位置:科研成果
撰稿人: 林垚 发布时间:2026-01-31
由于人体是一个整体系统,任何疾病进展不单单由发病器官本身决定,单独研究一个器官的疾病容易盲人摸象,跨器官通讯和跨分子调控在疾病中发挥重要作用。而计算生物学和多组学大数据分析对于研究系统性疾病具有天然优势。如何开发有效的计算方法和计算管线对系统性疾病进行新的理论解析越发重要。
2026年1月20日,我校安三奇团队在综合期刊Nature Communications上在线发表了题为“Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation”的研究性论文。该研究通过之前开发的机器学习算法scm6A,结合公开数据库数据和小鼠模型多组学数据分析,发现禁食可在Tp53驱动的胶质瘤模型中显著延缓肿瘤生长,而这一抗肿瘤效应与禁食诱导的肠道菌群重塑密切相关,其通过调控甲硫氨酸代谢水平,进一步影响RNA甲基化(N⁶-甲基腺苷,m6A)修饰状态,从而抑制肿瘤相关信号通路(TGF-β),从而实现跨器官信号传递。
该研究从饮食干预、肠道微生态与表观转录调控的交叉视角,揭示了肿瘤代谢调节的新机制,为探索低成本、低负担的肿瘤辅助治疗策略提供了重要实验依据,并为未来开展精准化、天然疗法干预研究奠定了理论基础。

具体分析如:小鼠m6A-seq显示Tp53-IF组的m6A修饰水平下降,且Tgfb2转录本上的甲基化饰显著减少。小鼠单细胞RNA测序共鉴定20类细胞群,肿瘤细胞可分为OPC-like、AC-like与MES-like 亚群。拟时序分析显示IF处理的肿瘤细胞趋向于终末状态,同时Mettl3与Tgfb2表达沿拟时序逐渐下降。小鼠单细胞m6A定量进一步证实 IF 在细胞水平显著降低m6A丰度,从而在单细胞维度上揭示了IF- m6A -TGF-β的调控关系。
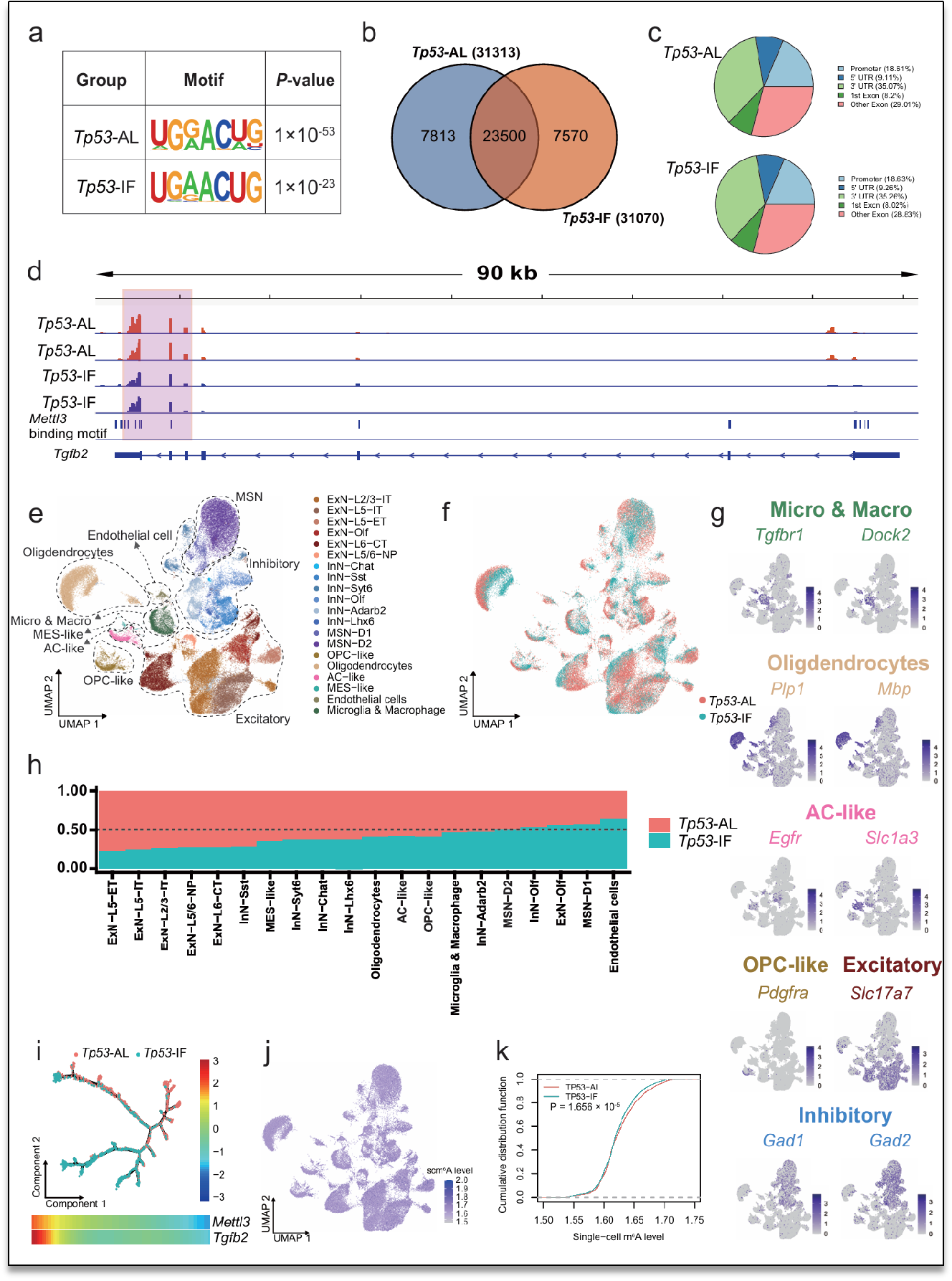
图1间歇性禁食在单细胞水平影响胶质瘤的m6A修饰
小鼠代谢组学显示Tp53-IF组中甲硫氨酸与S-腺苷甲硫氨酸(SAM)显著下降,并富集于半胱氨酸/甲硫氨酸代谢通路。小鼠空间代谢组与空间转录组联合分析发现,在Tp53-AL组肿瘤区域中SAM、Mettl3与Tgfb2 均高度富集,而IF明显削弱其在肿瘤区域的空间分布。多区域聚类结果表明,SAM-METTL3-TGF-β 轴在肿瘤空间异质性中具有核心作用,为IF通过代谢-表观转录调控抑制肿瘤提供空间证据。
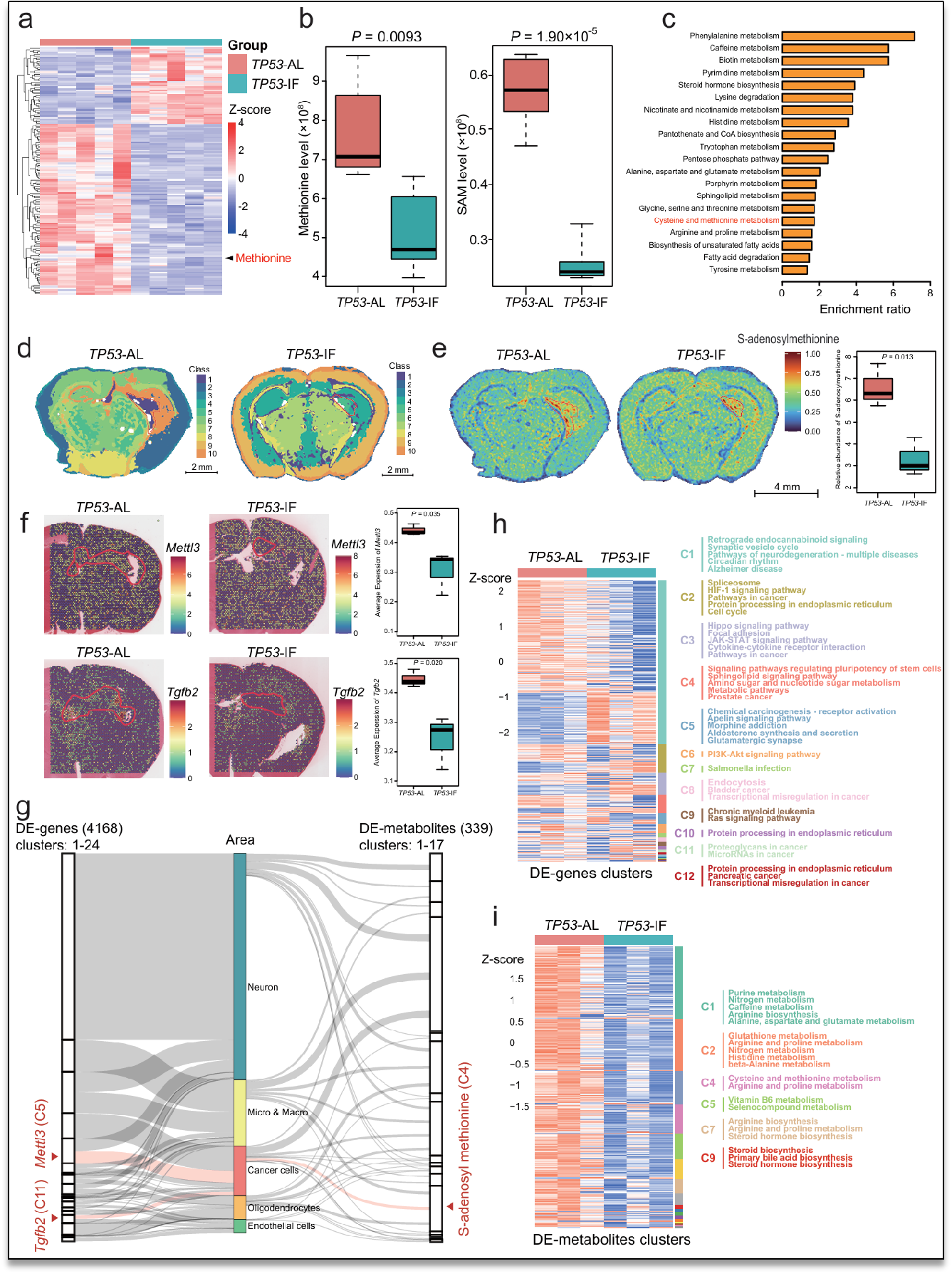
图2 空间组学联合分析揭示间歇性禁食调控甲硫氨酸–m6A信号轴
小鼠宏基因组测序显示IF显著改变Tp53 GBM小鼠肠道菌群结构,多个与甲硫氨酸合成相关的菌群(如 Alistipes、Prevotella 等)在IF条件下显著下降。功能注释与代谢通路富集分析进一步表明,IF 下调了与甲硫氨酸代谢及肿瘤相关的微生物功能模块。菌群-代谢物相关性分析证实,甲硫氨酸水平与多种关键菌属呈显著正相关,提示IF通过肠道菌群抑制甲硫氨酸供给。
文章结论与讨论,(未来)启发与展望
研究开发新的计算管线系统,利用公开组学数据和自测组学数据10种(单细胞转录组,单细胞甲基化,空间代谢组,空间转录组,bulk水平的宏基因组,Rip-seq测序,转录组,基因组,代谢组,蛋白组)揭示禁食对胶质瘤具有明显的基因型依赖性抑瘤效应,其疗效主要体现在TP53亚型。机制上,间歇性禁食通过重塑肠道菌群,抑制甲硫氨酸代谢,降低m6A修饰并抑制TGF-β信号通路,从而延缓肿瘤进展。总之,本研究通过新的机器学习管线和计算生物学发现天然疗法的抗癌效果要根据肿瘤亚型决定。
原文链接 https://www.nature.com/articles/s41467-026-68512-2
广西医科大学生科院硕士林垚(名额限制目前前往重庆医科大学攻读博士学位)主要撰写本新闻稿,他也是论文的第一作者,广西医科大学生科院安三奇为论文的通讯作者。该研究受广西八桂青年拔尖人才项目、广西医科大学杰出青年,以及自身筹措费用的支持。
安三奇近5年在PNAS,Nature Communication,Nucleic Acids Research,Cell Reports等国际权威期刊发表一系列论文,指导本科生和硕士作为第一作者在多篇顶刊发表高质量论文。目前团队高新招聘全职博士后(必须全职,而且脚踏实地,熟悉算法和编程)。博后邮件联系1721967953@qq.com。对生物信息和跨器官通信感兴趣的欢迎联系读博士后。